电话:15160017041邮箱:imtda321@qq.com

虽然三甲评审条款中没有关于医疗器械分类分级的明确字眼,但如要做到做好相关条款的要求,笔者认为,对医疗器械的“分类分级”势在必行!结合目前广大医疗机构内部医学装备管理部门的现状,“分类分级”做的好与否,也会直接或间接影响到医疗器械管理工作的效果。

医疗器械管理分类分级严格讲,涉及到研发、临床试验、制造、使用等各个环节,今天我们主要就“临床使用”这一环节进行探讨。
为此,我们尝试从“为什么这样做?”、“怎么做?”、“做到什么样”三方面谈谈一点微薄的见解,欢迎各位前辈同道留言批评指正,感谢!
医疗器械定义
参考中华人民共和国卫生行业标准《医疗器械安全管理》(全文阅读:http://imtda.com/Ne_d_gci_60_id_317.html),对医疗器械定义如下:

一、为什么这么做
■ 国家相关法规文件要求
(一)根据《医疗器械监督管理条例》(国务院,2021年2月)中“第六条:国家对医疗器械按照风险程度实行分类管理。”

(二)根据《医疗器械临床使用管理办法》(国家卫健委,2021年3月)中“第六条:医疗机构应当根据国家发布的医疗器械分类目录,对医疗器械实行分类管理。”
■ 意义
(一)医疗器械具有多学科覆盖、知识密集型的特点,涉及机械、电子、材料、生命科学等众多学科,既具有很强的专业性,又具有跨专业的综合性。医疗器械产品众多,组成各异,风险跨度大,从最简单的纱布、棉签,到植入人体支持生命的心脏起搏器、血管支架等,都属于医疗器械。
医疗器械的这些特点,决定了应当实行分类管理,以符合医疗器械的客观规律和发展要求。(以上内容引自书籍《医疗器械临床使用管理办法释义》,国家卫健委医政医管局 编)

(二)结合目前广大医学装备管理部门的一大现状:人员短缺,及医护老师的一大特点:临床工作繁忙。通过实行“分类分级”管理、“区别对待”,做到做好医疗器械管理。
二、怎么做
■ 国家相关文件指导
(一)国家市场监督管理总局于2015年分布了医疗器械分类规则,用于指导制定医疗器械分类目录和确定新的医疗器械的管理类别,对分类做了详尽的描述和指导。
全文阅读:http://imtda.com/Ne_d_gci_60_id_335.html。

(二)国家药监局于2023年发布关于进一步加强和完善医疗器械分类管理工作的意见。细化分类原则要求;修订完善分类目录。
全文阅读:http://imtda.com/Ne_d_gci_60_id_284.html。
■ 执行层面
(一)在“智管行”线上验收建账时,同时采用两种分类:(68分类方式暂不考虑)
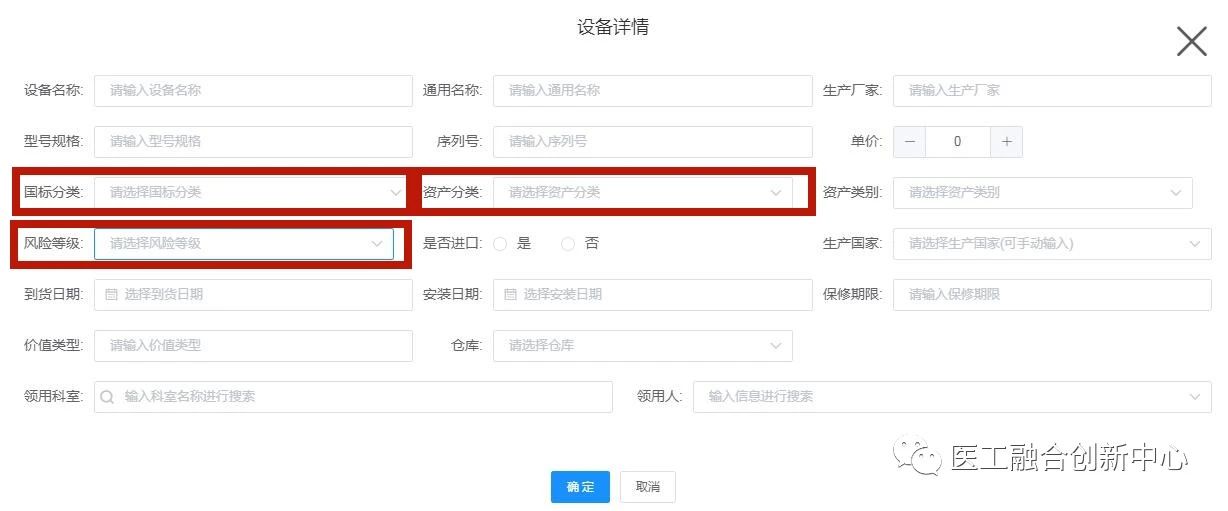
1、国标分类=政府采购品目分类目录(2022年印发)中医疗设备分类,与财务划分并轨。
下载请登网页:http://imtda.com/Ne_d_gci_60_id_335.html。
2、资产分类=医疗器械分类目录(2023版)。
下载请登网页:http://imtda.com/Ne_d_gci_60_id_335.html。

并根据《医疗器械安全管理》附录B.医疗器械风险等级分类,进行风险等级选择:三级高风险、二级中风险、一级低风险。
同时,也可以参考谢松城教授书籍《医疗设备使用安全风险管理》中的风险评估办法。

(二)在“智管行”质控中心做三级保养和巡检时,引入医疗器械分类分级,对高中低风险医学装备采用不同的处理方式。

接下来考虑在培训工作、调配中心库存设备安排等方面也需考虑进去医疗器械分类分级,高风险的一定要加强培训。
三、做到什么样
通过分类分级,在医院三级管理制度的框架下,让管理部门有的放矢、临床医护老师能抓住重点,即大家能较清晰清楚怎么做如何做,这样才能切实地把管理工作有效推动下去,实实在在地满足相关法规文件和《福建省医学装备管理质量控制检查评价标准》等要求后。
那么,三甲评审条款中的“加强医学装备安全管理,有明确的医疗器械临床使用安全控制与风险管理工作制度与流程。建立医疗器械临床使用安全事件监测与报告机制。”;“建立保障医学装备处于完好状态的制度与规范,对用于急救、生命支持系统仪器装备要始终保持在待用状态,建立全院应急调配机制。”等条款自然会满足。
更重要的是,可以真正地把医院医疗器械临床使用管理体系搭建起来,可以帮助真正实现加强医疗器械临床使用管理,保障医疗器械临床使用安全、有效的最终目标。
以上内容不足之处请各位前辈同道留言批评指正,也期待能与各位前辈同道探讨,共同提升。
来源:医工融合创新中心
医工融合创新中心编辑:蒋琴(实习生)
医工融合创新中心审核:朱宗达
欢迎关注医工融合创新中心公众号,一起探讨学习交流。

